कैसे की महान कहानी दिमित्री इवानोविच मेंडेलीव तालिका का पहला संस्करण प्रकाशित किया जो मौजूद सब कुछ बताता है।
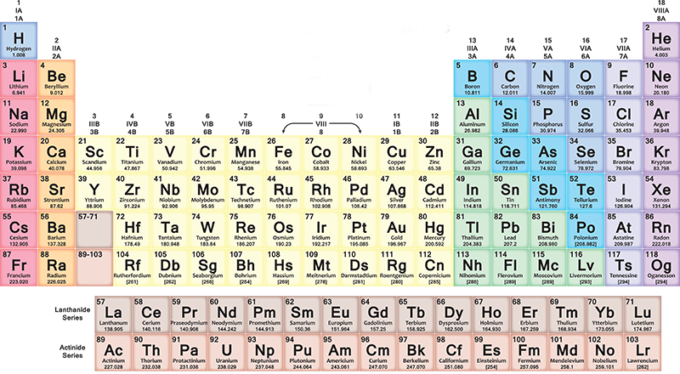
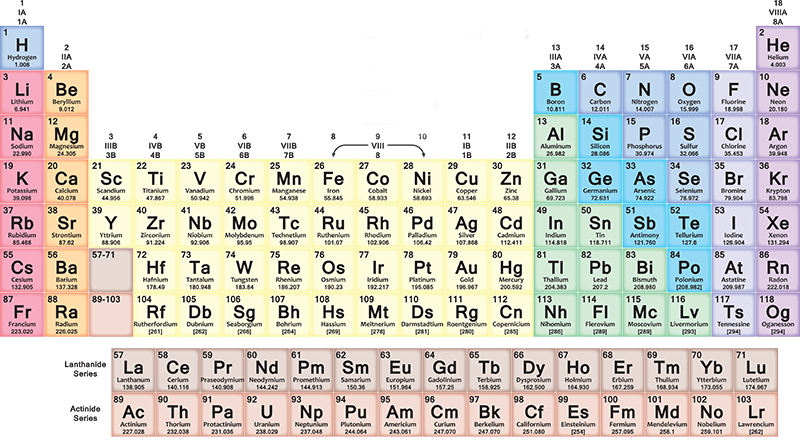
हर साल, दुनिया भर में हाई स्कूल के लाखों छात्र खुद को अक्षरों और संख्याओं से भरी एक रंगीन मेज के सामने पाते हैं, जो किसी तरह पूरे ब्रह्मांड को बताती है। हम कौन हैं और सब कुछ किस चीज से बना है, इसकी यह गवाही तत्वों की आवर्त सारणी है, जो 2019 में 150 साल की हो गई।
यह रूसी रसायनज्ञ थे दिमित्रिज इवानोविच मेंडेलीव जिन्होंने ऑक्सीजन, कार्बन, लोहा और अन्य सभी तत्वों को व्यवस्थित करने का एक तरीका खोजा - और अभी भी खोजा जाना है - उन्हें वर्गीकृत करने के लिए एक तालिका में। उनकी अंतर्दृष्टि को पहली बार 6 मार्च, 1869 को सार्वजनिक किया गया था, लेकिन आवर्त सारणी का इतिहास बहुत पहले शुरू हुआ था, और यह इस बारे में बहुत कुछ कहता है कि वैज्ञानिक जाँच कैसे काम करती है - जिस तरह से हम दुनिया को समझने की कोशिश करते हैं।
लवॉज़ियर की सूची
विज्ञान के अधिकांश इतिहासकार XNUMXवीं शताब्दी के अंत में फ्रांसीसी रसायनशास्त्री एंटोनी-लॉरेंट डी लावोइसियर द्वारा किए गए अध्ययनों में आवर्त सारणी की उत्पत्ति का पता लगाते हैं। एक बहुत बुरे अंत से पहले, फ्रांसीसी क्रांतिकारी अदालत द्वारा मौत की सजा सुनाई गई, लेवोज़ियर अपने समय के वैज्ञानिक अनुसंधान में कुछ सबसे महत्वपूर्ण प्रगति के लिए जिम्मेदार थे। अपनी पत्नी मैरी-ऐनी के साथ मिलकर उन्होंने तत्वों के अध्ययन के लिए कई साल समर्पित किए।: ऑक्सीजन और कार्बन जैसे पदार्थ जिन्हें अन्य पदार्थों में रासायनिक प्रतिक्रिया द्वारा "विघटित" नहीं किया जा सकता है। लेवोज़ियर ने द्रव्यमान के संरक्षण के कानून के पहले संस्करण को भी समझा, यह समझने के बाद कि रासायनिक प्रतिक्रिया में प्रारंभिक पदार्थों के वजन का योग प्रतिक्रिया के बाद प्राप्त पदार्थों के बराबर होना चाहिए।
एन 1789, ळवोइसिएर एक प्रारंभिक सूची प्रकाशित की 33 तत्वों में से उस समय तक पहचाने गए, यह जानते हुए कि शायद और भी बहुत कुछ खोजा जाना बाकी था (उनकी सूची आज ज्ञात लोगों का पांचवां हिस्सा दिखाती है)। सोना, लोहा और गंधक प्राचीन काल से ज्ञात हैं, जबकि अन्य की खोज हाल ही में हुई है। हालांकि अधूरी, सूची तत्वों को क्रम में रखने का पहला प्रयास था, एक बहुत ही जटिल पहेली जिसे हल करने में एक सदी से अधिक समय लगेगा और इसके लगभग सभी टुकड़ों को पूरा करने में कई और दशक लगेंगे।

प्राउस्ट और डाल्टन
अपनी सूची के प्रकाशन के पांच साल बाद, लेवोज़ियर को लोगों की क्रांतिकारी अदालत ने मौत की सजा सुनाई और उसका सिर कलम कर दिया गया। यह 1794 था, उसी वर्ष एक और वैज्ञानिक, लुइस-जोसेफ प्राउस्ट, वह इस निष्कर्ष पर पहुंचे थे कि यदि लेवोज़ियर का संरक्षण कानून मान्य था, तो "निश्चित अनुपात" से संबंधित एक नया टुकड़ा जोड़ा जाना था। प्राउस्ट ने 1799 में अपना नया कानून प्रतिपादित किया: जब दो या दो से अधिक तत्व एक यौगिक बनाने के लिए एक दूसरे के साथ प्रतिक्रिया करते हैं, तो वे हमेशा निश्चित और स्थिर द्रव्यमान अनुपात के अनुसार मिश्रित होते हैं.
हालांकि उनके कानून ने सुझाव दिया कि रासायनिक यौगिकों को अलग-अलग वजन के कणों से बना होना चाहिए, प्रत्येक एक दिए गए तत्व के कारण होता है। ब्रिटिश वैज्ञानिक थे जॉन डाल्टन (जिनके लिए हम "कलर ब्लाइंडनेस" शब्द का श्रेय देते हैं: जो कुछ रंगों को नहीं देख सकते थे और इस स्थिति के मुख्य छात्रों में से एक थे) जिन्होंने XNUMX वीं शताब्दी की शुरुआत में प्रदर्शित किया कि जब दो तत्व मिलकर यौगिक बनाते हैं, तो एक तत्व की मात्रा उन मात्राओं के साथ संयोजित होता है जो एक दूसरे के गुणक हैं, जो एक दूसरे से छोटी पूर्ण संख्याओं के रूप में संबंधित हैं।
मूल रूप से, अगर मैं 12 ग्राम कार्बन को 16 ग्राम ऑक्सीजन के साथ मिलाता हूं, तो मुझे कार्बन मोनोऑक्साइड (CO) मिलता है, लेकिन अगर मैं पूर्व को दोगुनी ऑक्सीजन के साथ मिलाता हूं, तो मुझे कार्बन डाइऑक्साइड (CO2) मिलती है। कार्बन के समान द्रव्यमान के साथ, कार्बन डाइऑक्साइड में कार्बन मोनोऑक्साइड की तुलना में दोगुनी ऑक्सीजन होती है। इससे यह अनुसरण करता है संयोजन अनुपात का मान आधा है.
मानव आंखों के लिए छोटी "चीजें", परमाणु
अपने नियम की व्याख्या करने के लिए, डाल्टन ने माना कि प्रत्येक तत्व मानव आँख के लिए अदृश्य छोटी चीज़ों से बना है, सभी का वजन समान है। उन्होंने उन्हें "परमाणु" कहा, कुछ अविभाज्य को परिभाषित करने के लिए ग्रीक शब्द का इस्तेमाल किया।

आदेश देना
कुछ ही वर्षों में लेवोजियर, प्राउस्ट और डाल्टन ने रसायन विज्ञान के तीन शास्त्रीय नियमों को औपचारिक रूप दिया था (वजन के नियम), वैज्ञानिक पद्धति की क्षमता का प्रदर्शन और दुनिया कैसे काम करती है, यह समझने के लिए एक मौलिक अनुशासन में तेजी से प्रगति, लेकिन इतनी सारी नवीनताओं के बीच आदेश देना आवश्यक था।
ऐसा करने वाले पहले स्वीडिश रसायनज्ञ थे जोन्स जैकब बर्जेलियस, जिन्होंने कार्बन के लिए "C" और आयरन के लिए "Fe" जैसे एक या दो अक्षरों का उपयोग करते हुए तत्वों के लिए संक्षिप्ताक्षर पेश किए। संक्षेप में उन्होंने विभिन्न तत्वों के अनुपात को इंगित करने के लिए संख्याओं को जोड़ा: जैसे एच में "2"2O, जो इंगित करता है कि हाइड्रोजन के दो भाग ऑक्सीजन के एक भाग से जुड़कर पानी के अणु का निर्माण करते हैं। वे अक्षर और संख्याएँ तत्वों की आवर्त सारणी पर समाप्त हो गए होंगे और आज भी आवश्यक हैं।
बर्ज़ीलियस काफ़ी रचनात्मक और जिज्ञासु व्यक्ति था।. इतालवी एलेसेंड्रो वोल्टा द्वारा आविष्कार की गई इलेक्ट्रिक बैटरी के बारे में जानने के बाद, जिसने रासायनिक प्रतिक्रिया के माध्यम से बिजली का उत्पादन किया, उसने विपरीत प्रभाव प्राप्त करने की कोशिश करने के लिए प्रयोग करना शुरू किया। उन्होंने समाधान में रासायनिक प्रतिक्रियाओं को प्रेरित करने के लिए बैटरी से बिजली का उपयोग किया, जिसे इलेक्ट्रोलिसिस कहा जाता है।
कई अन्य वैज्ञानिकों द्वारा अपनाई गई यह तकनीक पहले अज्ञात रासायनिक तत्वों की एक विस्तृत विविधता की खोज में सहायक साबित हुई। कुछ वर्षों के भीतर, ऐसे तत्वों की पहचान की गई जिनका अस्तित्व अब हमेशा के लिए मान लिया गया है, जैसे कि सोडियम, मैग्नीशियम, पोटेशियम और कैल्शियम। लेवोज़ियर द्वारा सूचीबद्ध तीस में दर्जनों नए तत्व जोड़े गए, जिसने नए प्रश्न खड़े किए: प्रकृति में वास्तव में कितने तत्व हैं? हम दूसरों को कैसे खोज सकते हैं? क्या ऐसे पदार्थ हैं जो हमें लगता है कि अन्य तत्वों के मिलन का परिणाम हैं और इसके बजाय वे स्वयं तत्व हैं?

आवर्त सारणी
जैसे-जैसे तत्वों की दौड़ जारी रही, कई वैज्ञानिक आश्चर्य करने लगे ऑर्डर कैसे करें और अपनी नई खोजों को कैसे समझें. ऐसा करने के लिए, आपको अलग-अलग पदार्थों की जांच करनी होगी और उनकी विशेषताओं की तुलना करनी होगी, सामान्य चीजों की तलाश करनी होगी। यह पता चला कि कुछ तत्वों को तिकड़ी में समूहीकृत किया जा सकता है और परमाणु भार द्वारा रैंक किया जा सकता है: केंद्र तत्व का वजन हमेशा उसके दो सबसे हल्के और सबसे भारी भागीदारों के बीच औसत वजन के बराबर होता है।
1860 के दशक की शुरुआत में, रसायनज्ञों के पास तीन मौलिक कानून, दर्जनों तत्व, उनमें से कुछ आवर्ती विशेषताओं का ज्ञान था, लेकिन उनके द्वारा खोजी गई दुनिया को नेविगेट करने के लिए कोई कैटलॉगिंग प्रणाली नहीं थी। केमिस्ट्री को क्रम में रखना लगभग एक जुनून बन गया था रूस में सेंट पीटर्सबर्ग विश्वविद्यालय में रसायन विज्ञान के प्रोफेसर: दिमित्री इवानोविच मेंडेलीव. फरवरी के अंत और मार्च 1869 की शुरुआत में, मेंडेलीव ने तत्वों की समझ बनाने के लिए काम किया। यह वस्तुतः एक सतत प्रतिबद्धता थी: उन्होंने दिन-रात काम किया, अंततः समय का ट्रैक खो दिया और बाद में कहा कि रसायन विज्ञान की पहेली को हल करने का अंतिम विचार एक संक्षिप्त सपने के बाद उनके पास आया था।
आवर्त सारणी का निर्माण
मेंडेलीव ने एक तालिका बनाई जिसमें तत्वों को एक सटीक मानदंड के अनुसार सूचीबद्ध किया गया था, जिसने इसकी विशेषताओं के बीच संबंधों को ध्यान में रखा। उनका सिस्टम पिछले प्रयासों से एक साधारण कारण से बेहतर था: यह अधिक ईमानदार था। दूसरे शब्दों में, इसने इस संभावना पर विचार किया कि खोजे जाने वाले अन्य तत्व भी थे और इसलिए, योजना के कुछ बक्सों का खाली होना सामान्य था। मेंडेलीव ने उन छेदों को छोड़ने के लिए बहुत आलोचना की, लेकिन बाद के दशकों की खोजें उन्हें सही साबित करेंगी।
तालिका ने न केवल नए तत्वों की खोज की संभावना पर विचार किया: यह भी सवाल किया कि क्या कुछ माप तब तक बने हैं उनमें से कुछ के बारे में सटीक थे। तालिका में, मेंडेलीव ने इस सिद्धांत का समर्थन करने वाले कुछ तत्वों को उल्टा कर दिया। कुछ मामलों में, अधिक सटीक मापों ने उन्हें सही साबित कर दिया, अन्य मामलों में नहीं, यह दिखाते हुए कि उस समय के वैज्ञानिक अभी भी परमाणु भार के बारे में कुछ याद कर रहे थे।

मेंडेलीव की तालिका का विकास
तत्वों की आवर्त सारणी की सुंदरता, संभवतः रसायनज्ञों की पसंदीदा ग्रिड, यह है कि यह एक समान पैटर्न की तरह नहीं दिखती है। कुछ पंक्तियों में कुछ आइटम हैं, जबकि अन्य 18 आइटम भरते हैं। इसे "आवधिक" कहा जाता है क्योंकि मेंडेलीव ने रासायनिक गुणों की पुनरावृत्ति का शोषण किया, समान रासायनिक विशेषताओं वाले तत्वों को समूहबद्ध किया।.
बाद के वर्षों में नए तत्वों की खोज के साथ, उस समय के लिए आश्चर्यजनक महान गैसों (जैसे हीलियम), निष्क्रिय और इसलिए पता लगाने में मुश्किल सहित, मेंडेलीव की तालिका तत्वों की एक सर्वव्यापी योजना को परिष्कृत करने के लिए एक दुर्जेय प्रारंभिक बिंदु साबित हुई, इसके बावजूद नई अंतर्दृष्टि और वैज्ञानिक साक्ष्य द्वारा लाई गई जटिलताएँ। उदाहरण के लिए, XNUMXवीं शताब्दी के अंत में, यह पता चला था कि परमाणु टुकड़े खो सकते हैं, यह सुझाव देते हुए कि वे स्वयं छोटे, अभी तक अनदेखे भागों से बने थे।
रासायनिक संरचना
एक बार फिर, कुछ दशकों में, रसायन विज्ञान ने छलांग और सीमाएं बनाईं, जिससे परमाणु संरचना के सिद्धांतों का निर्माण हुआ। उन्होंने उन चीजों की खोज की जिन्हें हम आज हल्के में लेते हैं, जैसे प्रोटॉन (धनात्मक आवेशित), न्यूट्रॉन (कोई आवेश नहीं) और इलेक्ट्रॉन (ऋणात्मक रूप से आवेशित) का अस्तित्व, वह है, उपपरमाण्विक घटक। इससे परमाणु संख्या का निर्धारण हुआ, जो एक परमाणु नाभिक में निहित प्रोटॉन की संख्या को इंगित करता है।
हालांकि, 1869 में कोई ज्ञान उपलब्ध नहीं होने के कारण, मेंडेलीव ने परमाणु भार पर अपनी योजना की व्यवस्था की थी (हालांकि समग्र लेआउट को फिट करने के लिए तत्वों के क्रम में कुछ प्रतिस्थापन के साथ)। अनजाने में, मेंडेलीव ने तत्वों को परमाणु संख्या के क्रम में व्यवस्थित किया था, वर्षों पहले इसी अवधारणा को पेश किया गया था। तालिका मूल्यों में परमाणु संख्याओं को प्रतिस्थापित करने से आवर्त सारणी के अंतिम अनुक्रम को जन्म मिला जिसे हम आज जानते हैं। परमाणु की संरचना की खोज के अलावा, 18वीं शताब्दी में क्वांटम यांत्रिकी ने आवर्त सारणी के और विकास और परिशोधन को जन्म दिया होगा, जो वर्तमान XNUMX-स्तंभ मॉडल में परिलक्षित होते हैं।
आवर्त सारणी कैसे बनाते हैं और कैसे पढ़ते हैं
आवर्त सारणी में, तत्वों को प्रत्येक पंक्ति (अवधि) में उत्तरोत्तर डाला जाता है उनके परमाणु क्रमांक के क्रम के अनुसार बाएं से दाएं: प्रत्येक नई पंक्ति एक नोबल गैस के बाद शुरू होती है। पंक्ति में पहला तत्व हमेशा एक क्षार धातु होता है, जिसकी परमाणु संख्या पिछली पंक्ति के साथ समाप्त होने वाले तत्व से अधिक होती है। अधिक सामान्यतः, तालिका की सात पंक्तियों में, धातु बाईं ओर होती है और अन्य प्रकार के तत्व दाईं ओर होते हैं।
इसलिए जैसे-जैसे आप दाहिनी ओर बढ़ते हैं आपको भारी और भारी वस्तुएँ मिलेंगी, धातु से गैस तक विभिन्न विशेषताओं के साथ। जब आप एक पंक्ति के अंत तक पहुँचते हैं और अगला प्रारंभ करते हैं, हमेशा बाएँ से दाएँ, वितरण चक्रीय रूप से दोहराया जाता है। सब कुछ एक निश्चित सामंजस्य के साथ लौटता है, जो आपको आश्चर्यचकित कर देगा यदि आप तालिका को देखकर पढ़ने का प्रयास करेंगे।
स्तंभों (समूहों या परिवारों) में समान रासायनिक विशेषताओं वाले तत्व होते हैं। उदाहरण के लिए, बाह्य इलेक्ट्रॉन विन्यास समान होता हैअर्थात्, इलेक्ट्रॉन जो अपने परमाणुओं के नाभिक के चारों ओर समान व्यवहार करते हैं। 18 समूह हैं और वे क्षार धातु समूह से लेकर नोबल गैस समूह तक हैं।
सभी तत्व प्राकृतिक नहीं होते
परमाणु संख्या 1 से 118 वाले तत्व आवर्त सारणी की सभी सात पंक्तियों में हैं: पहले 94 सभी प्राकृतिक हैं, जबकि 95 से 118 कृत्रिम रूप से प्राप्त किए गए हैं. नई वस्तुओं को विकसित करने के लिए अनुसंधान अभी भी प्रगति पर है, साथ ही योजनाबद्ध के वर्तमान लेआउट में हल किए जाने वाले कुछ मुद्दे भी हैं।
कुछ बदलावों के बावजूद, अपने 150 वर्षों के अस्तित्व में समग्र रूप से, तत्वों की आवर्त सारणी न केवल उन तत्वों को व्यवस्थित करने के लिए आवश्यक साबित हुई है, जो इन शब्दों को पढ़ने के लिए आपके द्वारा उपयोग की जाने वाली आँखों सहित, लेकिन यह भी प्रतिक्रियाओं के रसायन विज्ञान का विश्लेषण करने के लिए, विभिन्न यौगिकों के बीच संबंधों की खोज करें और परमाणु भौतिकी का अध्ययन करें। तालिका की पंक्तियाँ और स्तंभ इस बात का एक अतुलनीय संश्लेषण है कि वैज्ञानिक अनुसंधान क्या था जिसने इसके निर्माण को संभव बनाया और एक निश्चित अर्थ में, क्या होगा।