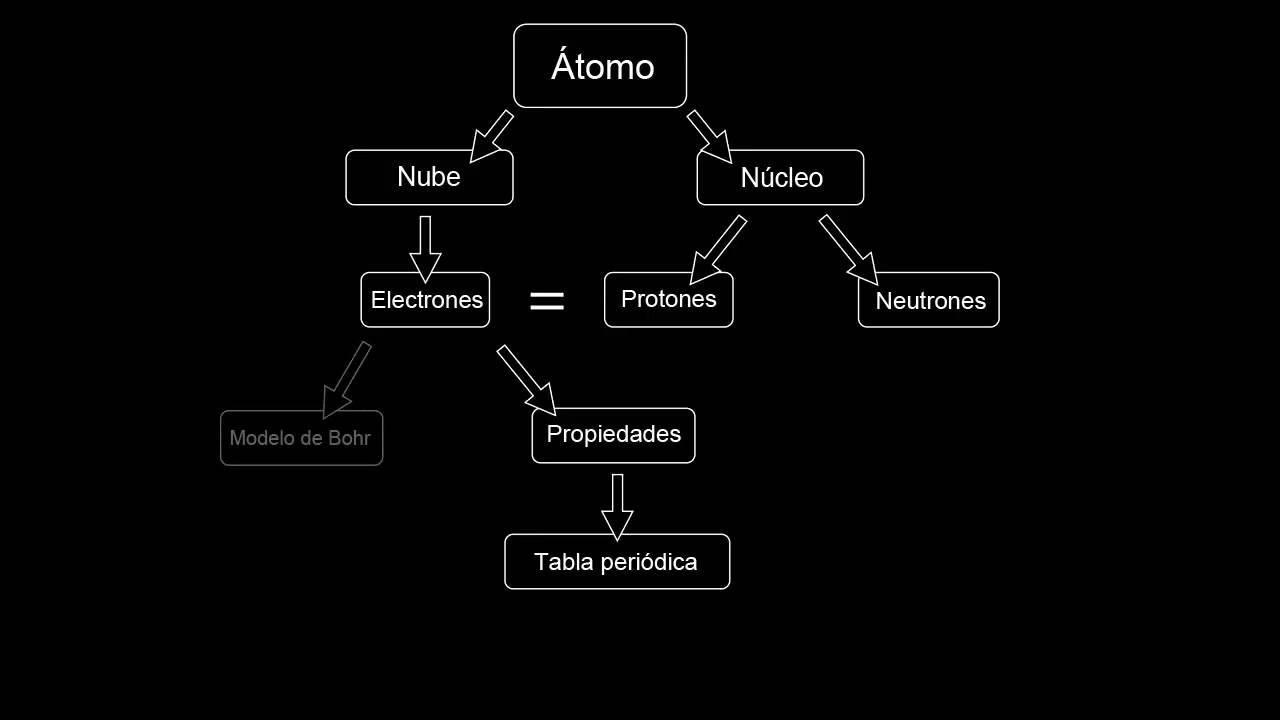
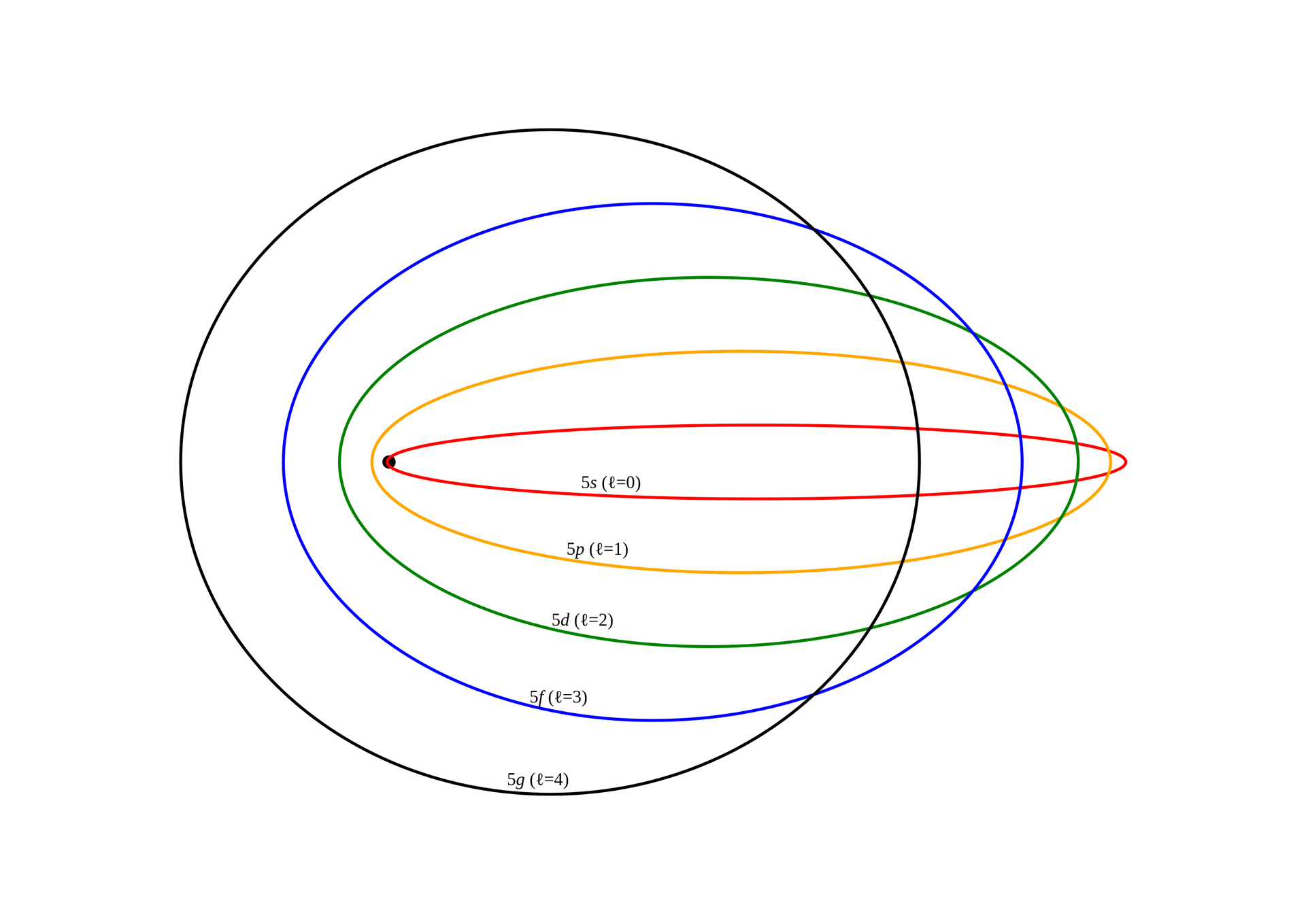
El Боров атомски модел покушајте да објасните како су елементи распоређени унутар атома. Са њим је било могуће закључити да је кретање атома по кружним орбитама и њихово померање између једне орбите и друге способно да произведе повећање или губитак енергије. Овде можете сазнати више о атомска теорија Боох.

Атомски Боров модел
Такође је добио име модела Рутхерфорд-Бохр. Развијен је 1913. године по Радерфордовом моделу, који је, иако успешан и револуционаран, имао извесних сукоба са Максвеловим и Њутновим законима, јер се долазило у обзир да су сви атоми нестабилни.
Радерфордов атомски модел заснивао се на чињеници да покретни електрони који имају негативан електрични набој треба да шире електромагнетно зрачење, у складу са законима електромагнетизма. Под претпоставком да је то тако, губитак енергије би проузроковао да електрони компримирају своју орбиту, спирално се крећући према центру атома, а затим колабирају у језгро.
Нове идеје
El Боров атомски модел дао решење за овај проблем, тврдећи да електрони круже по орбити око језгра, али само у неким дозвољеним орбитама и са одређеном енергијом која је пропорционална Планковој константи.
Ове дозвољене орбите су добиле назив енергетских шкољки или енергетских нивоа. То значи да енергетски капацитет електрона унутар атома није континуиран, већ се квантификује на одређеном нивоу.
Ови нивои се поистовећују са квантним бројем н (н = 1, 2, 3 и више) и према Бору, тај квантни број би се могао утврдити коришћењем Рибергове формуле, што је правило које је 1888. године створио шведски физичар Јоханес Риберг. да представи таласне дужине спектралних линија многих хемијских елемената.
Овај образац енергетских нивоа указивао је на то да електрони могу само да повећају или смање своју енергију ако успеју да скоче са једне орбите на другу, а када се то догоди, електрон би зрачио или апсорбовао електромагнетно зрачење у процесу.
El Боров атомски модел то је била модификација Радерфордовог модела. Из тог разлога су се задржале особености малог централног језгра са највећим делом масе. На исти начин, електрони су вршили своје орбитално кретање око језгра, на сличан начин као и планете око Сунца, али њихова орбитална кретања нису била равна.
Основни принципи Боровог атомског модела
Наелектрисане честице са електричном енергијом позитивног предзнака налазе се у веома малим количинама, ако их упоредимо са запремином атома и обухватају највећи део масе атома. Док се електрони, који имају негативан електрични набој, крећу око језгра по кружним орбитама, које већ имају унапред одређену величину и енергију. Због тога не постоје у средњем положају између орбита.
Енергија орбите је пропорционална њеној величини. Најмања енергија се налази у орбити са најмањим периметром. Што је енергетски ниво удаљенији од језгра, то је већа количина енергије коју поседује.
Различити нивои енергије имају различит број електрона. Што је ниво енергије нижи, то има мање електрона. На пример, на нивоу 1 биће до 2 електрона, на нивоу 2 ће бити до 8 електрона, итд. Дакле, енергија се зрачи или апсорбује у тренутку када електрон прелази из једне орбите у другу.
Додатна разматрања Боровог атомског модела
Разлог за постојање Боров атомски модел је да објасни да материја остаје стабилна, што претходни атомски модели нису чинили, као и спектри апсорпције и зрачења гасова.
Бор је први користио концепт квантизације, који га ставља између модела класичне механике, као што је Прилози Блеза Паскала и квантномеханички модел. Он је унапредио Ратерфордов модел укључивши открића квантизације која је направио Макс Планк неколико година раније и теорије Алберта Ајнштајна.
Упркос својим недостацима, Боров атомски модел био је претходник рођења квантне механике коју су покренули Шредингер и други научници, као и Планкова квантна теорија.
Ограничења и грешке у Боровом моделу
Модел не објашњава зашто су електрони јединствено ограничени на одређене орбите.
У моделу је наведено да електрони имају познати полупречник и орбиту, што ће Вернер Хајзенбергов принцип несигурности оповргнути десет година касније.
El Боров атомски модел имао је способност да репродукује понашање електрона у атомима водоника, али његови обрасци нису били применљиви на атоме других елемената који су имали већи број електрона.
Овај атомски модел представља недоследности када је у питању објашњење Зеемановог ефекта. Овај ефекат се може видети када се спектралне линије поделе на две или више, у присуству спољашњег и непокретног магнетног поља.
Исто тако, Боров атомски модел даје погрешну вредност за орбитални угаони момент материје у основном стању.
Сви ови разлози довели су до Боров атомски модел Годинама касније замењена је квантном теоријом, производом научног рада Хајзенберга и Шредингера.
Ко је био Ниелс Бохр?
Ниелс Бор је био физичар рођен у граду Копенхагену у Данској у октобру 1885. Његов отац је био универзитетски професор, а мајка кћерка богате породице. Имао је прилику да упише Универзитет у Копенхагену 1903. године, како би студирао физику, али је студирао и астрономију и математику. Године 1911. успео је да стекне звање доктора.
Такође 1911. године, захваљујући стипендији Карлсберг фондације, која је своје ресурсе посветила проучавању атома, успео је да отпутује у Лондон и током свог боравка упознаје релевантне научнике, као што су Џеј Џеј Томсон и Ернест Радерфорд.
Године 1912. вратио се у Данску, оженивши се Маргрете Норлуд, са којом је имао шесторо деце, од којих је једно постало реномирани физичар који је 1975. добио Нобелову награду, баш као што је то учинио његов отац годинама раније.
Основан у Данској и због непопуларности физике у својој земљи, био је приморан да предаје студентима медицине, што је била чињеница која није задовољила Бора, касније се вратио у Манчестер, у Енглеској, где му је Радерфорд понудио позицију. У Лондону је остао до 2 године након почетка Првог светског рата.
директора за физику и Нобелову награду
Године 1916. постављен је за директора теоријске физике на Универзитету у Копенхагену, што је била позиција створена посебно за њега. Године 1918. убедио је владу да оснује Дански институт за теоријску физику, данас познат као Институт Ниелс Бор, који је започео своје путовање 1921. године, са њим као главним директором.
Добио је Нобелову награду за физику 1922. за свој рад у истраживању атома и зрачења које емитују. Затим, 1924. године, Бор је упознао Хајзенберга у Данској и касније је имао прилику да прими научнике као што су Паул Дирац и Ервин Сцхродингер, који су могли да обликују размишљање и тумачење квантне механике у Копенхагену.
Бор је умро 18. новембра 1962. у Карлсбергу у Данској, али је био отац модерне физике у својој земљи.
Надамо се да ће ово читање на Боров атомски модел је било занимљиво и позивамо вас да сазнате више о нашим научним садржајима.