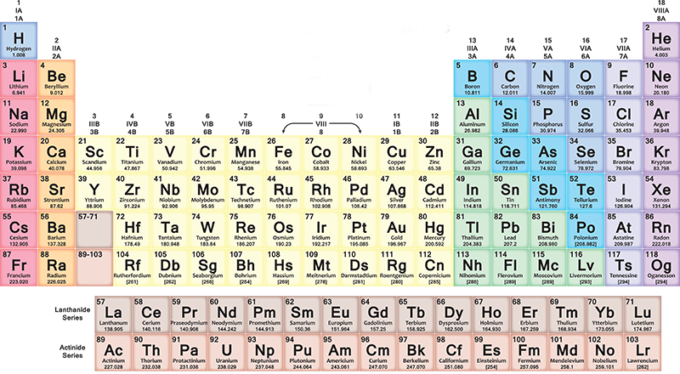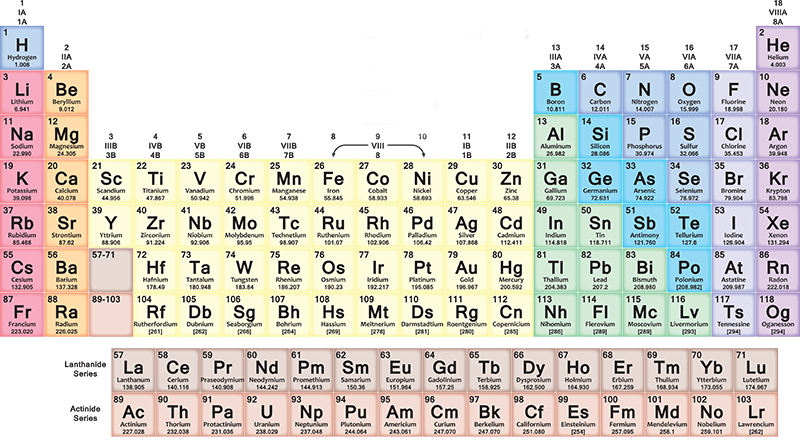
Kisah hebat bagaimana Dmitry Ivanovich Mendeleev menerbitkan versi pertama jadual yang menerangkan semua yang wujud.
Setiap tahun, berjuta-juta pelajar sekolah menengah di seluruh dunia mendapati diri mereka berada di hadapan meja berwarna-warni, penuh dengan huruf dan nombor, yang entah bagaimana memberitahu seluruh alam semesta. Kesaksian tentang siapa kita dan dari apa semuanya dibuat adalah jadual unsur berkala, yang pada tahun 2019 berusia 150 tahun.
Ia adalah ahli kimia Rusia Dmitriy Ivanovich Mendeleev yang menemui cara untuk memesan oksigen, karbon, besi dan semua unsur lain yang ditemui -dan masih akan ditemui- dalam jadual untuk mengelaskannya. Wawasannya mula-mula didedahkan kepada umum pada 6 Mac 1869, tetapi sejarah jadual berkala bermula lebih awal, dan ia banyak menceritakan tentang cara siasatan saintifik berfungsi—cara kita cuba memahami dunia.
senarai Lavoisier
Kebanyakan ahli sejarah sains mengesan asal usul jadual berkala kepada kajian yang dijalankan oleh ahli kimia Perancis Antoine-Laurent de Lavoisier pada akhir abad ke-XNUMX. Sebelum menemui akhir yang sangat buruk, dijatuhi hukuman mati dengan memenggal kepala oleh mahkamah revolusi Perancis, Lavoisier bertanggungjawab untuk beberapa kemajuan terpenting dalam penyelidikan saintifik pada zamannya. Bersama isterinya Marie-Anne, dia menumpukan bertahun-tahun untuk mengkaji unsur-unsur.: Bahan seperti oksigen dan karbon yang tidak boleh "terurai" oleh tindak balas kimia kepada bahan lain. Lavoisier juga menyatakan versi pertama undang-undang pemuliharaan jisim, selepas memahami bahawa dalam tindak balas kimia jumlah berat bahan awal mestilah sama dengan bahan yang diperoleh selepas tindak balas.
Dalam 1789 lebih lavoisier menerbitkan senarai awal daripada 33 elemen dikenal pasti sehingga masa itu, mengetahui bahawa mungkin terdapat banyak lagi yang perlu ditemui (senarainya menunjukkan kira-kira satu perlima daripada yang diketahui hari ini). Emas, besi dan sulfur telah diketahui sejak zaman purba, manakala yang lain telah ditemui lebih baru-baru ini. Walaupun tidak lengkap, senarai itu adalah percubaan pertama untuk menyusun elemen, teka-teki yang sangat rumit yang akan mengambil masa lebih daripada satu abad untuk diselesaikan dan banyak lagi dekad untuk diselesaikan dengan hampir semua bahagiannya.

Proust dan Dalton
Lima tahun selepas penerbitan senarainya, Lavoisier dijatuhi hukuman mati oleh mahkamah revolusi rakyat dan dipenggal kepalanya. Ia adalah 1794, tahun yang sama bahawa seorang saintis lain, Louis-Joseph Proust, dia telah membuat kesimpulan bahawa jika undang-undang pemuliharaan Lavoisier adalah sah, maka bahagian baharu yang berkaitan dengan "kadaran pasti" perlu ditambah. Proust menyatakan undang-undang barunya pada tahun 1799: apabila dua atau lebih unsur bertindak balas antara satu sama lain untuk membentuk sebatian, ia sentiasa sebatian mengikut perkadaran jisim yang pasti dan tetap..
Walaupun undang-undangnya mencadangkan bahawa sebatian kimia mesti dibuat daripada zarah-zarah yang berlainan berat, setiap satunya boleh dikaitkan dengan unsur tertentu. ialah saintis British John dalton (kepada siapa kita berhutang istilah "buta warna": yang tidak dapat melihat beberapa warna dan merupakan salah seorang pelajar utama keadaan ini) yang menunjukkan pada awal abad ke-XNUMX bahawa apabila dua unsur bergabung untuk membentuk sebatian, kuantiti unsur adalah bergabung dengan kuantiti yang gandaan antara satu sama lain, yang berkaitan antara satu sama lain sebagai nombor bulat kecil.
Pada asasnya, jika saya menggabungkan 12 gram karbon dengan 16 gram oksigen, saya mendapat karbon monoksida (CO), tetapi jika saya menggabungkan bekas dengan dua kali lebih banyak oksigen, saya mendapat karbon dioksida (CO2). Dengan jisim karbon yang sama, karbon dioksida mengandungi dua kali lebih banyak oksigen daripada karbon monoksida. Daripada ini ia mengikuti itu nilai nisbah gabungan ialah separuh.
"Benda" kecil pada mata manusia, atom
Untuk menjelaskan undang-undangnya, Dalton menganggap bahawa setiap elemen terdiri daripada benda-benda kecil yang tidak dapat dilihat oleh mata manusia, semuanya mempunyai berat yang sama. Dia memanggil mereka "atom", mengambil perkataan Yunani yang digunakan untuk mentakrifkan sesuatu yang tidak boleh dibahagikan.

meletakkan pesanan
Dalam beberapa tahun Lavoisier, Proust dan Dalton telah memformalkan tiga undang-undang klasik kimia (undang-undang berat), menunjukkan potensi kaedah saintifik dan kemajuan pesat dalam disiplin asas untuk memahami bagaimana dunia berfungsi, tetapi ia adalah perlu untuk mengatur di antara begitu banyak perkara baru.
Antara yang pertama melakukan ini ialah ahli kimia Sweden Jons Jacob Berzelius, yang memperkenalkan singkatan untuk unsur, menggunakan satu atau dua huruf seperti "C" untuk karbon dan "Fe" untuk besi. Pada singkatan dia menambahkan nombor untuk menunjukkan perkadaran pelbagai elemen: seperti "2" dalam H2O, yang menunjukkan dua bahagian hidrogen bergabung dengan satu bahagian oksigen untuk membentuk molekul air. Huruf dan nombor tersebut akan berakhir pada jadual unsur berkala dan masih penting hari ini.
Berzelius adalah seorang yang kreatif dan ingin tahu.. Selepas mengetahui tentang bateri elektrik yang dicipta oleh Alessandro Volta Itali, yang menghasilkan elektrik melalui tindak balas kimia, dia mula bereksperimen untuk cuba mendapatkan kesan sebaliknya. Dia menggunakan elektrik daripada bateri untuk mendorong tindak balas kimia dalam larutan, dipanggil elektrolisis.
Teknik ini, yang diguna pakai oleh beberapa saintis lain, terbukti memainkan peranan penting dalam menemui pelbagai jenis unsur kimia yang tidak diketahui sebelum ini. Dalam beberapa tahun, unsur-unsur yang kewujudannya kini nampaknya sentiasa dipandang remeh, seperti natrium, magnesium, kalium dan kalsium, telah dikenal pasti. Puluhan elemen baharu telah ditambahkan pada tiga puluh yang disenaraikan oleh Lavoisier, yang menimbulkan persoalan baharu: Berapa banyak unsur yang terdapat dalam alam semula jadi? Bagaimanakah kita boleh menemui orang lain? Adakah terdapat bahan yang kita fikir adalah hasil daripada penyatuan unsur lain dan sebaliknya adalah unsur itu sendiri?

jadual berkala
Apabila perlumbaan untuk unsur-unsur berterusan, ramai saintis mula tertanya-tanya cara memesan dan memahami penemuan baharu anda. Untuk melakukan ini, anda perlu memeriksa bahan individu dan membandingkan ciri-ciri mereka, mencari perkara yang sama. Telah didapati bahawa beberapa unsur boleh dikumpulkan kepada trio dan disusun mengikut berat atom: unsur tengah sentiasa mempunyai berat yang sama dengan berat purata antara dua pasangannya yang paling ringan dan paling berat.
Pada awal 1860-an, ahli kimia mempunyai tiga undang-undang asas, berpuluh-puluh unsur, pengetahuan tentang beberapa ciri berulang di kalangan mereka, tetapi tiada sistem pengkatalogan untuk mengemudi dunia yang mereka temui. Mengatur kimia menjadi hampir obsesi untuk a profesor kimia di Universiti Saint Petersburg di Rusia: Dmitry Ivanovich Mendeleev. Pada akhir Februari dan awal Mac 1869, Mendeleev berusaha untuk memahami unsur-unsur. Ia benar-benar komitmen berterusan: dia bekerja siang dan malam, akhirnya kehilangan jejak masa dan kemudian mengatakan bahawa idea muktamad untuk menyelesaikan teka-teki kimia telah datang kepadanya selepas mimpi singkat.
Penciptaan jadual berkala
Mendeleev mencipta jadual di mana unsur-unsur telah disenaraikan mengikut kriteria yang tepat, yang mengambil kira hubungan antara ciri-cirinya. Sistemnya lebih baik daripada percubaan sebelumnya untuk satu sebab mudah: ia lebih jujur. Dalam erti kata lain, beliau memikirkan kemungkinan terdapat unsur-unsur lain yang boleh ditemui dan oleh itu, adalah perkara biasa untuk beberapa kotak dalam skema itu kosong. Mendeleev mendapat banyak kritikan kerana meninggalkan lubang tersebut, tetapi penemuan dekad berikutnya akan membuktikan dia betul.
Jadual itu bukan sahaja memikirkan kemungkinan untuk menemui unsur-unsur baru: turut mempersoalkan sama ada beberapa ukuran yang dibuat sebelum itu tentang sebahagian daripada mereka adalah tepat. Dalam jadual, Mendeleev menyongsangkan beberapa elemen yang menyokong teori ini. Dalam sesetengah kes, ukuran yang lebih tepat membuktikan dia betul, dalam kes lain tidak, menunjukkan bahawa saintis pada masa itu masih kehilangan sesuatu tentang berat atom.

Evolusi jadual Mendeleev
Keindahan jadual berkala unsur, mungkin grid kegemaran ahli kimia, ialah ia tidak kelihatan seperti corak seragam. Sesetengah baris mempunyai segelintir item, manakala yang lain diisi dengan 18 item. Ia dipanggil "berkala" kerana Mendeleev mengeksploitasi pengulangan sifat kimia, mengumpulkan unsur-unsur dengan ciri kimia yang serupa..
Dengan penemuan unsur-unsur baru pada tahun-tahun berikutnya, termasuk gas mulia yang mengejutkan pada masa itu (seperti helium), lengai dan oleh itu sukar untuk dikesan, jadual Mendeleev membuktikan titik permulaan yang menggerunkan untuk memperhalusi skema elemen yang merangkumi semua, walaupun komplikasi yang dibawa oleh pandangan baharu dan bukti saintifik. Pada akhir abad ke-XNUMX, sebagai contoh, didapati bahawa atom boleh kehilangan kepingan, menunjukkan bahawa mereka sendiri terdiri daripada bahagian yang lebih kecil, yang belum diperhatikan.
struktur kimia
Sekali lagi, dalam beberapa dekad, kimia membuat lompatan dan sempadan, membawa kepada perumusan teori struktur atom. Mereka menemui perkara yang kita ambil mudah hari ini, seperti kewujudan proton (bercas positif), neutron (tiada cas) dan elektron (bercas negatif), iaitu komponen subatom. Ini membawa kepada penentuan nombor atom, yang menunjukkan bilangan proton yang terkandung dalam nukleus atom.
Walau bagaimanapun, tidak mempunyai pengetahuan yang tersedia pada tahun 1869, Mendeleev telah mengatur skemanya pada berat atom (walaupun dengan beberapa penggantian dalam susunan unsur-unsur untuk menjadikan susun atur keseluruhan sesuai). tanpa sengaja, Mendeleev telah menyusun unsur mengikut urutan nombor atom, bertahun-tahun sebelum konsep ini diperkenalkan. Menggantikan nombor atom ke dalam nilai jadual menghasilkan urutan akhir jadual berkala yang kita ketahui hari ini. Sebagai tambahan kepada penemuan struktur atom, pada abad ke-18 mekanik kuantum akan menimbulkan evolusi lanjut dan penambahbaikan jadual berkala, yang dicerminkan dalam model XNUMX lajur semasa.
Cara membuat dan membaca jadual berkala
Dalam jadual berkala, unsur-unsur dimasukkan secara progresif dalam setiap baris (tempoh) dari kiri ke kanan mengikut urutan nombor atomnya: setiap baris baru bermula selepas gas mulia. Unsur pertama dalam baris sentiasa logam alkali, dengan nombor atom satu lebih besar daripada unsur yang berakhir dengan baris sebelumnya. Secara umum, dalam tujuh baris meja, logam berada di sebelah kiri dan jenis unsur lain berada di sebelah kanan.
jadi semasa anda bergerak ke kanan anda akan menemui barang yang lebih berat dan lebih berat, dengan ciri yang berbeza daripada logam kepada gas. Apabila anda sampai ke penghujung baris dan memulakan baris seterusnya, sentiasa dari kiri ke kanan, pengedaran diulang secara kitaran. Segala-galanya kembali dengan keharmonian tertentu, yang akan mengejutkan anda jika anda cuba membaca jadual dengan melihatnya.
Lajur (kumpulan atau keluarga) mengandungi unsur-unsur dengan ciri kimia yang serupa. Sebagai contoh, mempunyai konfigurasi elektron luar yang sama, iaitu, elektron yang berkelakuan dengan cara yang sama di sekeliling nukleus atomnya. Terdapat 18 kumpulan dan ia terdiri daripada kumpulan logam alkali hingga kumpulan gas mulia.
Tidak semua unsur adalah semula jadi
Unsur dengan nombor atom 1 hingga 118 menduduki kesemua tujuh baris jadual berkala: 94 yang pertama semuanya semula jadi, manakala 95 hingga 118 telah diperoleh secara buatan. Penyelidikan untuk membangunkan item baharu masih dalam proses, serta terdapat beberapa isu yang perlu diselesaikan dalam susun atur semasa skema.
Walaupun terdapat beberapa perubahan, secara keseluruhan dalam 150 tahun kewujudannya, jadual unsur berkala telah terbukti penting bukan sahaja untuk menyusun elemen yang membentuk semuanya, termasuk mata yang anda gunakan untuk membaca perkataan ini, tetapi juga untuk menganalisis kimia tindak balas, temui hubungan antara sebatian yang berbeza dan belajar fizik nuklear. Baris dan lajur jadual adalah sintesis yang tiada tandingan tentang penyelidikan saintifik yang membolehkan penciptaannya dan, dalam erti kata tertentu, apa yang akan berlaku.