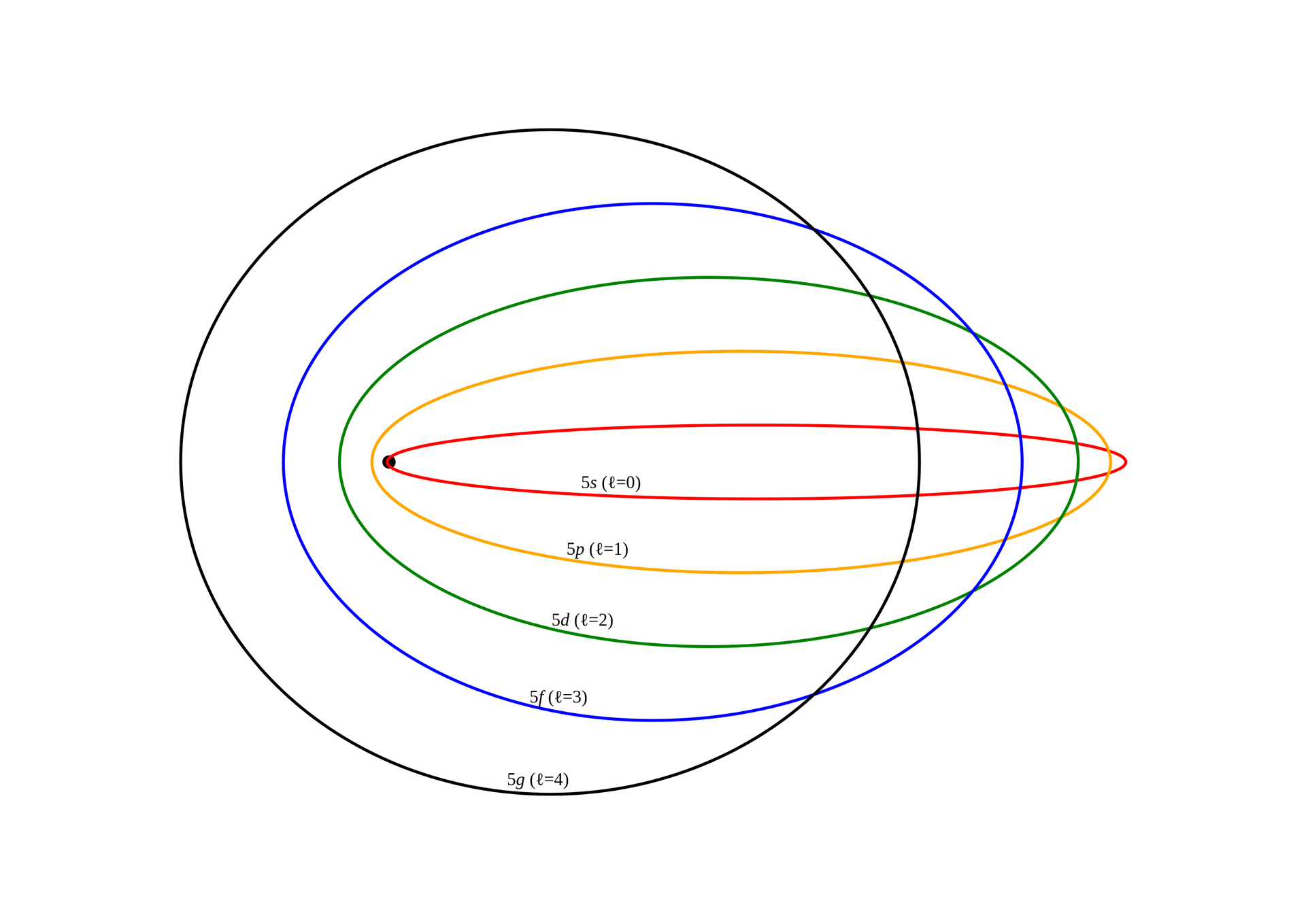
El Bohr atommodel prøv at forklare, hvordan grundstofferne er arrangeret i et atom. Med det var det muligt at udlede, at bevægelsen af atomer i cirkulære baner og deres forskydning mellem en bane og en anden var i stand til at producere stigninger eller tab af energi. Her kan du lære mere om atomteori af Båh.

Atomic Bohr model
Den fik også modelnavnet Rutherford-Bohr. Den blev udviklet i 1913, baseret på Rutherfords model, som, selvom den var vellykket og revolutionær, havde nogle konflikter med Maxwells love og Newtons love, fordi den kom til den betragtning, at alle atomer var ustabile.
Rutherfords atommodel var baseret på det faktum, at bevægelige elektroner, der havde en negativ elektrisk ladning, skulle udbrede elektromagnetisk stråling i henhold til elektromagnetismens love. Hvis det antages, at dette var tilfældet, ville tabet af energi få elektronerne til at komprimere deres bane, spiral mod atomets centrum og derefter kollapse ind i kernen.
Nye ideer
El Bohr atommodel gav løsningen på dette problem og argumenterede for, at elektronerne cirkulerer i kredsløb omkring kernen, men kun i nogle tilladte baner og med en vis energi, der er proportional med Plancks konstant.
Disse tilladte baner fik navnet energiskaller eller energiniveauer. Det betyder, at energikapaciteten af en elektron inde i et atom ikke er kontinuerlig, men kvantificeres på et vist niveau.
Disse niveauer er identificeret med et kvantetal n (n = 1, 2, 3 og mere), og ifølge Bohr kunne dette kvantetal etableres ved hjælp af Ryberg-formlen, som er en regel oprettet i 1888 af den svenske fysiker Johannes Ryberg at repræsentere bølgelængderne af spektrallinjerne for mange kemiske grundstoffer.
Dette mønster af energiniveauer indikerede, at elektroner kun kan stige eller falde i deres energi, hvis de formår at hoppe fra en bestemt bane til en anden, og når dette sker, ville elektronen udstråle eller absorbere elektromagnetisk stråling i processen.
El Bohr atommodel det var en modifikation af Rutherfords model. Af den grund bestod de særlige kendetegn ved en lille central kerne med det meste af massen. På samme måde lavede elektronerne deres banebevægelser rundt om kernen, på samme måde som planeterne omkring solen, men deres banebevægelser var ikke flade.
Grundlæggende principper for Bohr-atommodellen
Ladede partikler med elektrisk energi med positivt fortegn findes i meget små mængder, hvis vi sammenligner dem med atomets volumen og omfatter den største del af massen af atomet. Mens elektronerne, som har en negativ elektrisk ladning, bevæger sig rundt i kernen i cirkulære baner, som allerede har en forudbestemt størrelse og energi. På grund af dette eksisterer de ikke i en mellemposition mellem banerne.
Banens energi har et forhold, der er proportionalt med dets størrelse. Den laveste energi findes i kredsløbet med den mindste omkreds. Jo længere væk et energiniveau er fra kernen, jo større mængde energi besidder den.
Forskellige energiniveauer har forskelligt antal elektroner. Jo lavere energiniveau, jo færre elektroner har det. For eksempel vil der i niveau 1 være op til 2 elektroner, i niveau 2 vil der være op til 8 elektroner, og så videre. Så energi udstråles eller absorberes i det øjeblik en elektron skifter fra en bane til en anden.
Yderligere Bohr-atommodelovervejelser
Grunden til at være Bohr atommodel skulle forklare, at stof forbliver stabilt, hvilket tidligere atommodeller ikke gjorde, samt gassers absorptions- og bestrålingsspektre.
Bohr's var den første til at bruge begrebet kvantisering, som placerer det mellem en model for klassisk mekanik, som f.eks. Bidrag af Blaise Pascal og en kvantemekanisk model. Han forbedrede Rutherfords model ved at inkorporere kvantiseringsopdagelser gjort af Max Planck et par år tidligere og Albert Einsteins teorier.
På trods af sine mangler er Bohr atommodel var forløberen til fødslen af kvantemekanikken initieret af Schrödinger og andre videnskabsmænd, såvel som Planks kvanteteori.
Begrænsninger og fejl i Bohr-modellen
Modellen forklarer ikke, hvorfor elektroner entydigt er begrænset til bestemte baner.
I modellen stod det, at elektronerne havde en kendt radius og kredsløb, hvilket Werner Heisenbergs usikkerhedsprincip ville modbevise ti år senere.
El Bohr atommodel det havde evnen til at reproducere elektronernes opførsel i brintatomer, men dets mønstre var ikke anvendelige for atomer af andre grundstoffer, der havde et større antal elektroner.
Denne atommodel præsenterede uoverensstemmelser, når det kom til at forklare Zeeman-effekten. Denne effekt er, hvad der kan ses, når spektrallinjerne er opdelt i to eller flere, i nærværelse af et eksternt og immobilt magnetfelt.
Ligeledes er Bohr atommodel leverer en fejlagtig værdi for det orbitale vinkelmoment af stof i grundtilstanden.
Alle disse grunde førte til Bohr atommodel Det blev år senere erstattet af kvanteteori, et produkt af Heisenbergs og Schrodinger's videnskabelige arbejde.
Hvem var Niels Bohr?
Niels Bohr var fysiker født i København i oktober 1885. Hans far var universitetsprofessor, og hans mor var datter af en velhavende familie. Han fik mulighed for at komme ind på Københavns Universitet i 1903, for at studere fysik, men han studerede også astronomi og matematik. I 1911 nåede han at opnå sin doktorgrad.
Også i 1911, takket være at have vundet et stipendium fra Carlsbergfondet, som dedikerede sine ressourcer til studiet af atomet, lykkedes det ham at rejse til London og under sit ophold mødte han relevante videnskabsmænd, såsom JJ Thomson og Ernest Rutherford.
I 1912 vendte han tilbage til Danmark og giftede sig med Margrethe Norlud, med hvem han fik seks børn, hvoraf den ene blev en anerkendt fysiker, der vandt Nobelprisen i 1975, ligesom hans far havde gjort det år tidligere.
Etableret i Danmark og på grund af fysikkens upopularitet i sit land, blev han tvunget til at undervise medicinstuderende, et faktum, der var utilfreds med Bohr, og vendte senere tilbage til Manchester, England, hvor Rutherford havde tilbudt ham en stilling. Han forblev i London indtil 2 år efter begyndelsen af Første Verdenskrig.
Direktør for fysik og nobelpris
I året 1916 blev han udnævnt til direktør for teoretisk fysik ved Københavns Universitet, hvilket var en stilling skabt specielt til ham. I 1918 overbeviste han regeringen om at oprette Dansk Institut for Teoretisk Fysik, i dag kendt som Niels Bohr Institutet, som begyndte sin rejse i 1921, med ham som hoveddirektør.
Han blev tildelt Nobelprisen i fysik i 1922 for sit arbejde med undersøgelsen af atomer og den stråling, de udsender. Så i 1924 mødte Bohr Heisenberg i Danmark og fik senere mulighed for at modtage videnskabsmænd som Paul Dirac og Erwin Schrödinger, der formåede at forme tænkningen og fortolkningen af kvantemekanikken i København.
Bohr døde den 18. november 1962 i Carlsberg, Danmark, men han var faderen til moderne fysik i sit land.
Vi håber, at denne læsning på Bohr atommodel har været interessant, og vi inviterer dig til at lære mere om vores videnskabelige indhold.